Sabatolimab di Novartis riceve da EMA la designazione di farmaco orfano per il trattamento delle sindromi mielodisplastiche (MDS)
La Commissione Europea (CE) ha concesso la designazione di farmaco orfano a sabatolimab (MBG453) per il trattamento delle sindromi mielodisplastiche (MDS), sulla base di dati clinici che mostrano un alto tasso di risposte in pazienti con MDS ad alto rischio che sono stati trattati con sabatolimab in combinazione con agenti ipometilanti (HMA).
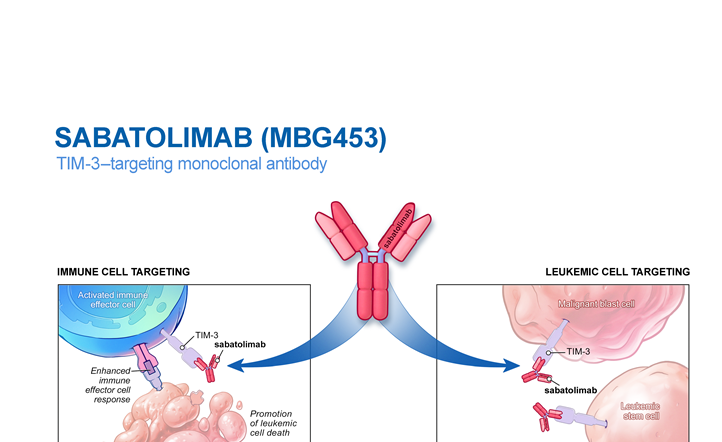
Sabatolimab è un potenziale nuovo capostipite di terapie immuno-mediate per il trattamento delle sindromi mielodisplastiche, avente come target il TIM-3, un nuovo bersaglio espresso dalle cellule immunitarie e leucemiche, ma non sulle normali cellule staminali ematopoietiche. Mirare a TIM-3 risveglia il sistema immunitario per attaccare selettivamente le cellule staminali leucemiche (responsabili di MDS e AML) e ha il potenziale per fornire una risposta duratura e con un buon profilo di tollerabilità.
Sabatolimab è in fase di sviluppo per il trattamento della sindrome mielodisplastica (MDS) ad alto rischio e della leucemia mieloide acuta (AML). Il programma di sviluppo comprende gli studi di Fase II STIMULUS-MDS1, di Fase III STIMULUS-MDS2, Fase II STIMULUS-MDS3 e Fase II STIMULUS-AML1.
Sabatolimab ha ottenuto, nel Maggio 2021, dalla Food and Drug Administration (FDA) la fast track designation in US per il trattamento di pazienti adulti con sindromi mielodisplastiche (MDS), definite con una categoria di rischio IPSS-R alto o molto alto, in combinazione con agenti ipometilanti. La designazione rapida facilita lo sviluppo e accelera l'iter autorizzativo.
